
|
|
 |
|
|
Construyendo un
espectroscopio .
|
||
|
|
Un espectroscopio es un aparato que permite descomponer la luz blanca en todos los colores que la componen y observarlos. En otro capítulo se menciona la descomposición de la luz blanca con un prisma (ver "Experimentos de física"). Ahora veremos como usar una red de difracción con el mismo propósito. Pero,como se consigue una red de difracción? Muy fácil: usamos un disco compacto o CD que ya no sirva. Veamos como conseguir las diferentes partes y como armar nuestro espectroscopio:
1)
La red de difracción. Utilizando una sierra
de dientes finos, debemos cortar una tira que puede tener el ancho del agujero
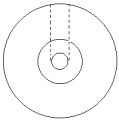 central del CD, aproximadamente (ver figura). Antes de cortar, conviene
proteger con cinta adhesiva (cinta "scotch") la parte que nos interesa,
para que no se raye demasiado. De un mismo disco podemos cortar varias tiras,
si queremos armar más de un espectroscopio.
central del CD, aproximadamente (ver figura). Antes de cortar, conviene
proteger con cinta adhesiva (cinta "scotch") la parte que nos interesa,
para que no se raye demasiado. De un mismo disco podemos cortar varias tiras,
si queremos armar más de un espectroscopio.
2) La caja del espectroscopio puede fabricarse con cartón grueso para que tenga cierta rigidez y deberá tener las medidas (en milimetros) que se indican en la figura:
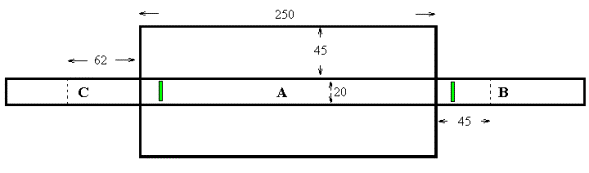
Luego de dibujar el esquema de la figura sobre el cartón, doblamos hacia abajo todas las partes, de manera que la parte marcada con A quede como lado superior de la caja. Si el cartón es realmente grueso (1 mm o algo así), conviene marcar los dobleces con una herramienta muy afilada para facilitar el doblado. Las partes B y C pueden ser tiras de cartón cortadas aparte y luego unidas a la parte A con cinta "scotch" (esas tiras deben tener la longitud necesaria como para cerrar la parte de abajo de la caja que se forma y deben ser dobladas por las líneas de puntos indicadas). En la parte A se deberá cortar con una herramienta bien afilada la abertura de entrada de la luz (indicada con color verde) que tendrá 12 x 3 mm y estará a unos 20 mm del borde más cercano. En la parte B se cortará la abertura de observación (también indicada en verde), con las mismas medidas que la anterior y a 12 mm del borde más cercano. Una vez hechos los dobleces, se deberá sujetar la “red de difracción” que ya preparamos a la parte interna de la parte C, como se indica en la figura siguiente, y ubicar esa parte formando un ángulo de 45º con el borde de la caja.
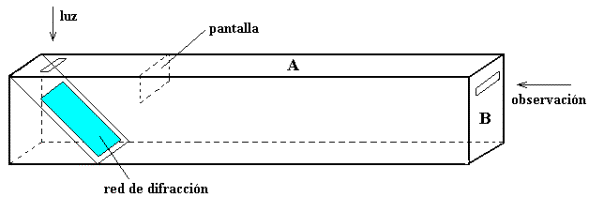
3) Rendija de entrada. La luz deberá entrar por una fina rendija de 10 mm de largo y 0,5 mm de ancho que deberá hacerse en un trocito de papel negro o cartón fino. Esa pieza se pega luego sobre la abertura cortada en la parte A (indicada con la flecha que dice “luz”). Además, se puede pegar un trocito de cartón (indicado como"pantalla" en la figura) en la parte interna de la parte A para que la luz que entra por la rendija no pueda verse directamente por la ventanita de observación cortada en B.
4) Tomando ahora nuestro espectroscopio de manera que la rendija de entrada esté bien iluminada por una lámpara eléctrica común o por la luz del cielo, al mirar por la ventana de observación deberíamos ver el espectro de la luz blanca, o sea todos los colores que forman la luz blanca (como en el arco iris), con los colores azul en la parte superior y rojo en la parte inferior. Se puede probar de cambiar un poco el ángulo de la red de difracción o la posición de la ventana de observación, tratando de obtener un espectro de mayor longitud y que se vea claramente.
Este aparatito nos permitirá determinar en que zonas del espectro emite luz o absorbe luz una sustancia. Podremos entonces hacer los siguientes experimentos:
a) Dirigiendo la rendija de entrada hacia un tubo fluorescente, veremos, además de los colores del espectro común, líneas brillantes de color amarillo, verde y azul, debidas al mercurio que estos tubos tienen en su interior. Es luz que emite el mercurio y por lo tanto lo denominamos espectro de emisión.
b) Ahora colocamos nuestro espectroscopio en un soporte adecuado e iluminamos la rendija de entrada con una lámpara eléctrica común (preferentemente de luz difusa, en las que no se puede ver el filamento incandescente) o con la luz del cielo en un día soleado (pero no directamente al Sol!). Luego colocamos entre la rendija y la luz un frasco de vidrio incoloro con el fondo más o menos plano (o una cápsula de Petri, que podemos pedir a algún bioquímico amigo). Con esta instalación podremos ver en que zona del espectro absorben luz las soluciones. Veremos entonces un espectro de absorción. Por ejemplo:
- Ponemos en el recipiente de vidrio una solución concentrada de sulfato de cobre (como la utilizada en "Experimentos de química"). Veremos que aparece una zona obscura en el espectro, lo que indica adonde está absorbiendo esa solución. El color celeste que tiene esta solución es debido a la luz que no es absorbida.
- Con una solución de permanganato de potasio (preguntar en una farmacia) muy diluída, que tiene un color rojo violáceo, se verá que pasa luz en las zonas del rojo y el azul, mientras que aparecen bandas de absorción en la zona del amarillo y el verde. Como se modifica el espectro de absorción con distintas concentraciones de la solución?
- También podemos probar con una solución de clorofila. Moliendo algunas hojas verdes (de perejil, por ejemplo) con un poco de alcohol fino y filtrando el líquido a través de papel (de filtro para café) o de un trozo de algodón, obtendremos una solución de color verde intenso.Con ayuda de nuestro espectroscopio veremos que esa solución absorbe en las zonas del azul y del rojo y deja pasar solamente luz verde, que le da el color a la solución.
Los que quieran perfeccionar el espectroscopio le pueden incorporar una escala de longitudes de onda de la luz. Para esa tarea convendrá guiarse por las longitudes de onda de las líneas que se ven en el espectro del mercurio, al observar la luz de un tubo fluorescente: línea amarilla en 579 nm, línea verde en 546 nm, línea azul en 436 nm, línea violeta en 405 nm.
Recordemos que las longitudes de onda de la luz están expresadas en nanometros, abreviado nm. Un nanometro es igual a 1 metro dividido por 1.000.000.000, o sea mil millones. Es realmente una longitud muy, muy pequeña!
![]()
La Página de la Ciencia.